meta data for this page
Verdampfungswärme
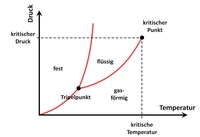
Für den Übergang vom flüssigen zu gasförmigen Aggregatzustand ist die zufuhr einer Energiemenge $Q_\mathrm{V}$ nötig, die als Verdampfungswärme bezeichnet wird. Dies wird beschrieben durch die Clausius-Clapeyron-Gleichung: $$Q_\mathrm{V}=\frac{\mathrm{d}p}{\mathrm{d}T}(V_\mathrm{D}-V_\mathrm{Fl})\,T \quad \left[\mathrm{J}\right] \, ,$$ mit $\frac{\mathrm{d}p}{\mathrm{d}T}$ der Steigung der Dampfdruckkurve $p_\mathrm{Dampf}(T)$, $V_\mathrm{D}$ dem Volumen des Dampfes, $V_\mathrm{Fl}$ dem Volumen der Flüssigkeit und $T$ der Temperatur während des Übergangs. Diese Gleichung lässt sich anders schreiben als $$\frac{\mathrm{d}p}{\mathrm{d}T}=\frac{Q_\mathrm{V}}{T}\frac{1}{V_\mathrm{D}-V_\mathrm{Fl}}=\frac{\Delta S}{\Delta V}\, ,$$ mit der Entropieänderung $\Delta S=\frac{Q}{T}$ und der Volumenänderung $\Delta V=V_\mathrm{D}-V_\mathrm{Fl}$.
Die Verdampfungswärme wird häufig mit $\Lambda$ bezeichnet und bezieht sich dann auf $1\,\mathrm{kg}$ Material das verdampft werden soll. Wenn der Dampf wieder kondensiert wird die Energiemenge $\Lambda$ als Kondensationsenergie wieder frei. Die molare Verdampfungswärme, also die Wärme die notwendig ist um ein Mol eines gewissen Stoffes zu verdampfen, errechnet sich, indem die Verdampfungswärme durch die Stoffmenge $n$ geteilt wird,
$$ Q_\mathrm{m} = \frac{Q}{n} \quad \left[\frac{\mathrm{J}}{\mathrm{mol}}\right] \, .$$
Herleitung der Clausius-Clapeyron-Gleichung
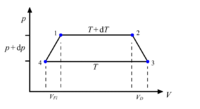
Zur Herleitung wird ein Kreisprozess betrachtet bei dem das Arbeitsmedium einer ständigen Phasen-Umwandung von flüssig zu gasförmig und zurück unterliegt.
In Zustand 1 ($T+\mathrm{d}T \, ,\, p+\mathrm{d}p$) ist das Arbeitsmedium kondensiert, also flüssig, und nimmt das Volumen $V_\mathrm{flüssig}$ ein.
Nun soll das Arbeitsmedium verdampft werden, dazu wird es mit einem Wärmebad der Temperatur $T+\mathrm{d}T$ in Kontakt gebracht und unter Aufnahme von Wärmeenergie $\Lambda$ vergrößert sich das Volumen auf $V_\mathrm{dampf}$ (1→2), dabei verdampft das Arbeitsmedium vollständig. Der Prozess leistet die Arbeit $$\Delta W_1 = -\left(p+\mathrm{d}p\right)\cdot\left(V_\mathrm{dampf}-V_\mathrm{flüssig}\right)\, .$$ Im nächsten Teilprozess (2→3) vergrößert sich das Arbeitsmedium durch eine adiabatische Expansion um einen als klein angenommenen Betrag. Druck und Temperatur verringern sich dabei um die als infinitesimal klein angesehenen Beträge $\mathrm{d}T$ und $\mathrm{d}p$.
Im Zustand 3 ($T \, ,\, p$) angelangt wird das Arbeitsmedium mit einem Wärmebad der Temperatur $T$ in Kontakt gebracht und es findet eine isotherme Kompression statt bis im Zustand 4 der Dampf wieder kondensiert ist (3→4). Dabei wird die externe Arbeit $$\Delta W_2=p\cdot\left( V_\mathrm{dampf}-V_\mathrm{flüssig} \right)$$ aufgewendet und die freiwerdende Energie $\mathrm{d}Q_\mathrm{ab}$ wird abgeführt. Als letzten Schritt findet wieder eine adiabatische Expansion statt, die ebenfalls als klein angenommen wird (4→1) und es findet eine infinitesimale Erhöhung von Temperatur und Druck statt.
Da die Prozess-Schritte (2→3) und (4→1) als vernachlässigbar angesehen werden, gilt $$\Delta W_\mathrm{ges}=\Delta W_1 + \Delta W_2 =-\mathrm{d}p\cdot\left( V_\mathrm{dampf}-V_\mathrm{flüssig} \right)\, .$$
Die Clausius-Clapeyron-Gleichung erhält man nun über den Wirkungsgrad $\eta$ durch $$\eta = -\frac{\Delta W}{|Q_{1->2}|}=\frac{\mathrm{d}p\cdot(V_\mathrm{dampf}-V_\mathrm{flüssig})}{\Lambda}=\frac{\mathrm{d}T}{T+\mathrm{d}T}\approx\frac{\mathrm{d}T}{T}\, .$$ $$ \frac{\mathrm{d}p\cdot(V_\mathrm{dampf}-V_\mathrm{flüssig})}{\Lambda}=\frac{\mathrm{d}T}{T} $$ $$ \Leftrightarrow Q_\mathrm{V}\equiv\Lambda = \frac{\mathrm{d}p\cdot(V_\mathrm{dampf}-V_\mathrm{flüssig}) T}{\mathrm{d}T\cdot\Lambda} $$ Dabei wurde ausgenutzt, dass $T\gg \mathrm{d}T$ und $|Q_{1->2}| = \Lambda.$